DEFINIZIONE DI INSONNIA
L’insonnia è definita come la ripetuta difficoltà ad iniziare, mantenere o consolidare il sonno e/o come la compromissione della qualità del sonno stesso che avvengono nonostante tempo ed opportunità di addormentamento siano adeguate.
Secondo il “Diagnostic and Statistical Manual of Mental Disorders” l’insonnia viene definita clinicamente come:
1)l’ insoddisfazione della quantità o qualità del sonno, con uno o più dei seguenti sintomi:
– Difficoltà ad iniziare il sonno
– Difficoltà a mantenere il sonno, con frequenti risvegli o difficoltà a riprendere il sonno
– Risveglio al mattino presto con impossibilità di riprendere il sonno
2) Il disturbo del sonno che causa significativo distress o altera almeno una delle seguenti attività quotidiane:
– Fatica o riduzione di energia
– Sonnolenza diurna
– Difficoltà a mantenere la concentrazione, l’attenzione o la memoria
– Disturbo dell’umore
– Difficoltà al comportamento quotidiano
– Alterazione delle normali attività quotidiane
– Alterazione delle normali attività sociali
– Influenza negativa riguardo i comportamento con il caregiver o la famiglia
3)un disturbo del sonno che perdura almeno 3 notti a settimana, presente per almeno 3 mesi, e che avviene nonostante vi siano adeguate occasioni per dormire
FISIOPATOLOGIA
L’insonnia spesso rappresenta il risultato dell’interazione tra fattori biologici, fisici, psicologici e ambientali. Nonostante un periodo transitorio di cattiva qualità del sonno possa colpire qualsiasi persona, l’insonnia vera e propria che perdura nel tempo sembra potersi sviluppare solo in uno specifico sottogruppo di persone che dimostrano una particolare predisposizione.
Ad evidenza di ciò è stato dimostrato come soggetti affetti da insonnia per lungo tempo abbiano:
-maggiore incidenza di depressione e ansia
-aumentato periodo di latenza del sonno
-metabolismo giornaliero aumentato
-maggiore variazione del sonno tra “notte e notte”
-attività beta all’elettroencefalogramma più rappresentata durante il sonno (un pattern osservato maggiormente durante processi di memorizzazione ed attività)
-aumento del consumo globale di glucosio al riscontro PET durante la transizione “veglia—> addormentamento”
In modelli da esperimento, soggetti sani sottoposti a deprivazione di sonno non hanno dimostrato le stesse anormalità nel metabolismo, nel sonno e nella personalità rispetto ai soggetti affetti da insonnia. Tuttavia se a questi soggetti veniva somministrata caffeina causando uno stato di ipereccitazione, il pattern metabolico, di sonnolenza diurna e di personalità assumeva caratteristiche del tutto simili a quelle dei soggetti affetti da insonnia.
A maggior sostegno della tesi dell’”ipereccitazione” si è visto come pazienti affetti da insonnia abbiano:
-aumento delle frequenze rapide durante il sonno NREM (il quale rappresenta un segno all’elettroencefalogramma di aumentata eccitazione cerebrale)
-ridotta disattivazione delle regioni sonno/veglia durante il sonno NREM
-aumento della temperatura corporea-aumento del cortisolo urinario-aumentata secrezione di adrenalina
-aumentati livelli di ACTH.
Questi risultati sembrerebbero supportare la teoria che il cattivo o assente riposo notturno potrebbe non essere la causa delle disfunzioni diurne, ma banalmente la manifestazione notturna di un disturbo più generalizzato.
Il modello di Spielman
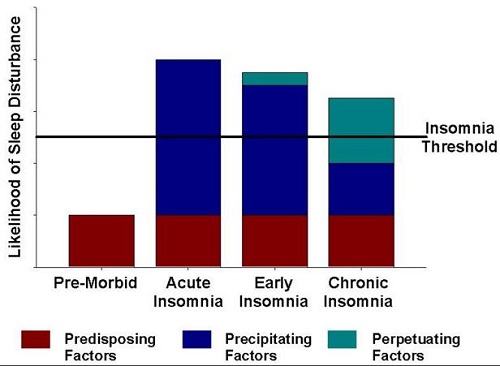
Il modello di Spielman dell’insonnia cronica parla di 3 componenti fondamentali: fattori predisponenti (genetici o familiari), fattori precipitanti (depressione, stress, ansia, condizioni lavorative o mediche ecc) e fattori perpetuanti (eccessiva preoccupazione per la qualità del sonno o per il sonno perso, sonnellini pomeridiani ecc). In accordo con questo modello i fattori predisponenti potrebbero essere la causa di occasionali episodi di insonnia, ma in generale questi soggetti hanno un corretto ritmo sonno-veglia fino a quando un evento precipitante (es. decesso di un caro) causa l’insorgenza acuta di insonnia. Se questa situazione si protrae nel tempo a causa di fattori perpetranti legati a cattive abitudini, l’insonnia diventa cronica e persiste nonostante la rimozione del fattori precipitante che l’ha scatenata.
EPIDEMIOLOGIA
In diversi studi le donne hanno riferito problemi di insonnia 1,4 volte maggiori rispetto agli uomini. Dati epidemiologici ci indicano come il 40% delle donne di età compresa tra 40 e 55 anni abbiano disturbo del sonno. L’insonnia protratta e cronica ha un frequenza età correlata ed è verosimilmente più rappresentata nell’età avanzata. La sua prevalenza aumenta dal 25% nella popolazione adulta a quasi il 50% nella popolazione anziana. Circa il 50% di coloro con diagnosi di insonnia hanno un disordine psichiatrico, e più frequentemente un disturbo dell’umore (depressione maggiore) o un disordine di ansia (disturbo di ansia generalizzato o disordine post-traumatico da stress). Diverse patologie risultano spesso associate all’insonnia, in particolar modo quelle che causano riduzione del respiro, dolore, nicturia, disturbi gastrointestinali o limitazione nella mobilità. L’insonnia primitiva, ovvero quella che non dimostra altre cause scatenanti di tipo secondario, rappresenta solo il 15% circa del totale delle cause.

Approssimativamente una persona su due di quelle che presentano sintomi severi hanno un andamento cronico. Il sintomo più comune è la difficoltà a mantenere il sonno (circa il 61% dei pazienti con insonnia), seguito dal risveglio precoce mattutino (52%) e dalla difficoltà nell’addormentamento (38%). Da notare come in circa la metà delle persone con insonnia vi siano almeno 2 di questi sintomi. Queste tipiche manifestazioni sovente cambiano nel tempo, ovvero una persona che inizialmente ha difficoltà ad addormentarsi può presentare successivamente difficoltà a mantenere il sonno, e viceversa.
PERCHE’ TRATTARE L’INSONNIA?
Il disturbo del sonno causa significativo distress e altera le normali attività quotidiane e questo è evidenti a tutti. L’insonnia prolungata però è anche risultata da alcuni studi fattore di rischio indipendente per alcune specifiche patologie. Una metanalisi di più di 20 studio di Baglioni C. et al ha concluso come l’insonnia persistente sia associata con raddoppio del rischio di incidenza di depressione maggiore. Come citato nell’articolo “Insomia Disorder” di John W. Et. Al del New England Journal of Medicine (2015) associazioni sono state anche riportate con un maggior rischio di IMA e CAD, scompenso cardiaco, ipertensione, diabete e morte, soprattutto se l’insonnia è accompagnata da una durata del sonno inferiore alle 6h per notte.
VALUTAZIONE
La valutazione clinica dell’insonnia necessita di una raccolta dei sintomi notturni e diurni,la loro durata, e la loro associazione temporale con elementi stressogeni psicologici e fisiologici. L’insonnia presenta molte manifestazioni, per cui è necessaria una completa valutazione che includa una anamnesi medica e psichiatrica, così come la valutazione di patologie che si associano specificatamente ai disturbi del sonno (es. OSAS o sindrome delle gambe senza riposo). E’ necessario richiedere al paziente comportamenti nelle ore precedenti all’addormentamento, ed ogni possibile elemento notturno che possa portare al risveglio ed interferire con il sonno. Mantenere per 2-4 settimane un diario del sonno che riporti l’ora in cui si va a letto, qualunque risveglio notturno ed il risveglio finale, può aiutare ad indentificare pattern irregolari di sonno.
NB: La polisonnografia non è indicata nella valutazione dell’insonnia a meno che non si sospetti OSAS o altre patologie specifiche.
Nell’inquadramento dell’insonnia è anche fondamentale:
1)somministrare il seguente questionario per comprendere la qualità del sonno notturno del paziente ed il livello di sonnolenza diurna:
Epworth sleepiness scale in italiano LINK
2)far compilare al paziente eventualmente facendosi aiutare da un caregiver un diario del sonno di almeno due settimane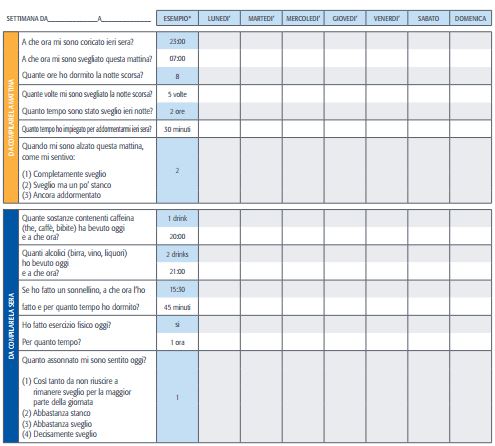
DIARIO DEL SONNO COMPLETO SCARICABILE in formato PDF al LINK
3) raccogliere la storia farmacologica del paziente facendo attenzione ai farmaci insonnia-correlati come Beta bloccanti, Clonidina, Teofillina (in particolare in acuto), Antidepressivi (in particolare fluoxetina), decongestionanti, OTC e rimedi erboristici.
GESTIONE TERAPEUTICA
TERAPIA COMPORTAMENTALE COGNITIVA (TCC)
La TCC è considerata la terapia di prima linea nel trattamento dell’insonnia. Viene usualmente effettuata singolarmente o in gruppo, per una durata di circa 6-8 incontri ed i benefici generalmente perdurano per circa 6-12 mesi (durata dimostrata superiore rispetto per esempio alla terapia con benzodiazepine dopo interruzione). L’aderenza alla TCC non è ottimale nella pratica clinica probabilmente perché viene richiesto un importante cambiamento nelle proprie abitudine (es. riducendo il tempo speso a letto ed alzandosi dal letto appena svegli) e l’ efficacia della terapia si manifesta solo dopo diverso tempo in attesa del quale vi sono spesso piccoli miglioramenti globali. Questo alimenta il pessimismo verso tali approcci da parte del paziente.
Elementi di terapia comportamentali cognitiva
Restrizione di sonno: stabilizzare il ritmo circadiano, riducendo il tempo in cui si rimane a letto
Controllo degli stimoli: ridurre gli elementi disturbanti e promuovere l’associazione tra letto e sonno
Terapia cognitiva: sfatare credenze sbagliate riguardo alle conseguenze sulla salute dell’insonnia mantenendo aspettative ragionevoli
Terapia rilassante: esercizi di meditazione o respiro
Igiene del sonno: limitare l’uso di caffeina ed alcool, tenere il letto al buio ed in ambiente silenzioso, evitare riposi diurni o serali, aumentare l’attività fisica (non troppo ravvicinato al momento del riposo), rimuovere orologi nella stanza da letto.
TERAPIE FARMACOLOGICHE

IPNOTICI NON BENZODIAZEPINICI: non sono strutturalmente delle benzodiazepine ma si legano ai recettori di queste ultime. Tutti riducono la latenza del sonno e sono approvati per l’uso nei pazienti con insonnia da addormentamento ed alcuni hanno dimostrato minore tolleranza rispetto agli agonisti benzodiazepinici.
Zopiclone: Primo ipnotico non benzodiazepinico ad essere utilizzato nella clinica. L’emivita di 5-7 h (intermedia) rende minimo l’accumulo dopo somministrazioni ripetute e minimi gli effetti residui al risveglio. Una sua peculiarità è quella di indurre “sapore metallico”. Utile sia come farmaco di “addormentamento” che principalmente come farmaco di “mantenimento” ha dimostrato basso potenziale di abuso. Data la scarsa tolleranza gli effetti terapeutici si sono rivelati prolungati (6-12 mesi) pur mantenendo un dosaggio costante. Picco plasmatico 1,5-2h. DOSE standard: 7,5 mg
Zaleplon: la farmacocinetica di questo farmaco ha due importanti e peculiari caratteristiche: l’assorbimento e l’eliminazione sono rapidissimi determinando un veloce inizio dell’attività farmacologica (1 h) e una totale assenza di effetti residui il giorno seguente. Non avendo metaboliti attivi l’emivita è brevissima (1h) . Queste caratteristiche lo rendono molto utile per le insonnie da addormentamento e per i risvegli notturni (se il risveglio mattutino è previsto almeno dopo 4h). L’efficacia di zaleplon si mantiene per 12 mesi. Non è risultato adatto in soggetti tolleranti alle benzodiazepine. DOSE standard: 10 mg.
Zolpidem: sebbene gli effetti di questo farmaco siano legati ad una interazione con il recettore delle benzodiazepine questa molecola possiede una attività sedativo-ipnotica a dosi molto inferiori rispetto a quelle necessarie per ottenere un effetto anticonvulsivante e miorilassante. Lo zolpidem ha scarsa tendenza ad indurre tolleranza anche dopo uso prolungato ma sviluppa dipendenza in modo simile alle benzodiazepine. Avendo un’emivita di 2,5 h, è molto utile per le insonnie di addormentamento e non causa sedazione mattutina. Zolpidem compresse sublinguali a basso dosaggio è l’unico approvato come farmaco per i risvegli notturni se il risveglio mattutino è previsto almeno dopo 4h. Picco plasmatico 1,5 h. DOSE standard: 10 mg.
NB: Zolpidem, zopiclone ed in minima parte lo Zaleplon sono metabolizzati dal CYP3A4.
IPNOTICI BENZODIAZEPINICI: a dosaggi opportuni producono effetti sedativo-ipnotici di intensità sufficiente a facilitare il sonno. In particolare questi farmaci diminuiscono il tempo necessario all’addormentamento (latenza), aumentano la durata totale del sonno e riducono drasticamente la durata dei microrisvegli (periodi di risveglio parziale che durano solo pochi secondi e di cui il paziente è ignaro). La scelta di una benzodiazepina particolare in questi disturbi è basata su criteri farmacocinetici.
Ai pazienti che faticano ad addormentarsi ed a quelli che devono essere vigli durante il giorno è consigliabile la somministrazione di benzodiazepine a breve durata d’azione:
Triazolam : emivita 1,5-5,5 h, picco plasmatico 0,5-2 h . DOSE standard: 125-250 mcg.
Brotizolam: emivita 3-8 h, picco plasmatico 45 min. DOSE standard: 0,25 mg.
Le molecole con emivita intermedia sono più adatte a soggetti che lamentano risvegli mattutini precoci:
Temazepam: emivita 9,5-12,4 h, picco plasmatico 2-3 h. DOSE standard: 10-20 mg
Estazolam: emivita 10-24 h, picco plasmatico 0,5-1,6 h. DOSE standard: 0,5-2 mg
Lorazepam: emivita 14 h, picco plasmatico 2 h. DOSE standard: 1-2,5 mg
Bromazepam: emivita 20,1 h, picco plasmatico 1,2 h. DOSE standard: 1,5- 3 mg.
Le molecole con emivita lunga andrebbero riservate ai pazienti con concomitante ansia diurna:
Diazepam: emivita 20-70 h, picco plasmatico 30-90 min. DOSE standard: 2-5 mg.
Flurazepam: emivita 48-120 h, picco plasmatico 0,5-3 h . DOSE standard: 15-60 mg
Nitrazepam: emivita 25-300 h, picco plasmatico 40-80 min . DOSE standard: 5 mg
Flunitrazepam: emivita 15-30 h, picco plasmatico 0,75-2 h . DOSE standard: 0,5-1 mg
Delorazepam: emivita 100 h, picco plasmatico 45-min1,5 h. DOSE standard: 0,5-1 mg
Clobazam: emivita >42h, picco plasmatico 0,5-4h. DOSE standard: 10 mg
Ketazolam: emivita 48h,picco plasmatci 3h. DOSE standard: 15-75 mg
La maggior parte di queste molecole ad eccezione di alcune (come lorazepam e temazepam) sono metabolizzate totalmente o in parte a livello del CYP3A4.
NB: Per tutti questi farmaci n caso di sospensione, è indicata una riduzione graduale e supervisionata (es. circa il 25% della dose di partenza ogni 2 settimane).
ATTENZIONE!
principali induttori del CYPA34 che quindi ridurranno l’efficacia di questi farmaci sono: rifampicina, carbamazepina, fenobarbital,fenitoina, hypericum, glucocorticoidi (desametasone)
principali inibitori che ne aumenteranno gli effetti sono : macrolidi (claritromicina, eritromicina), antifungini azolici (itraconazolo,ketoconazolo,fluconazolo) ciprofloxacina, metadone, succo di polmpelo, antidepressivi (fluoxetina,paroxetina, sertralina, venlafaxina), cimetidina.
MELATONINA: ormone secreto fisiologicamente dalla ghiandola pineale. La concentrazione di questa molecola è maggiore nel sangue durante il sonno notturno e minore durante la veglia diurna.

Molti studi riguardo alla melatonina hanno una durata limitata e le evidenze sono risultate conflittuali. Tuttavia sembrerebbe fondamentale la tempistica con cui questo ormone viene somministrato al fine di ottenere l’effetto biologico. La somministrazione da 30 minuti prima fino a 2 ore per le compresse a rilascio modificato (uniche disponibili in Europa) sembrerebbe l’unica modalità in grado di garantire una probabile efficacia. La melatonina assunta al momento di coricarsi non ha dimostrato successo terapeutico. In uno studio del 2010 Wade et al hanno ottenuto risultati nella riduzione della latenza del sonno e nella durata totale in soggetti con più di 65 anni per un tempo pari a 6 mesi. Per questi motivi la melatonina nell’insonnia è indicata in soggetti con età superiore a 55 anni. DOSE standard: 2 mg.
CURIOSITA‘: Il ramelteon è un agonista del recettore della melatonina recentemente approvato dalla FDA per il trattamento dell’insonnia non disponibile in Italia.
Farmaci off-label per l’insonnia
Antidepressivi (trazodone, mirtazapina, amitriptilina): L’uso di antidepressivi con effetto sedativo per trattare l’insonnia trae vantaggio dall’attività antistaminergica, anticolinergica, serotoninergica e adrenergica di questi principi attivi. Alle basse dosi con cui vengono comunemente usati per l’insonnia, hanno scarso effetto antidepressivo o ansiolitico. Benchè le evidenze a supporto di questi agenti farmacologici non siano vaste, il trazodone è usato come agente ipnoinducente in circa il 1% degli adulti americani, generalmente ad un dosaggio dai 25mg ai 100mg. La mirtazapina presenta efficacia antidepressiva ed ansiolitica alle dosi usati per l’insonnia e rappresenta ragionevolmente la prima opzione per i pazienti con patologie coesistenti; bisogna ricordare che la mirtazapina può determinare incremento ponderale.
Antipsicotici (quetiapina , ziprasidone e olonzapina): efficaci per l’insonnia ma gli effetti collaterali importanti e relativamente frequenti rendono difficoltoso l’uso di questo farmaco per il trattamento esclusivo.
NB: spesso sono necessari piani terapeutici per la prescrizione
Terapia negli anziani
La qualità e quantità di sonno declinca con l’avanzare dell’età. Questo risulta probabilmente correlato a meccanismi fisiologici dell’invecchiamento quali la diminuzione del sonno ad onde lente (“sonno profondo”), con conseguente facile risvegliabilità e difficoltà a riprendere sonno. A questo si aggiunge l’abitudine a svegliarsi molto presto al mattino e ad addormentarsi altrettanto presto la sera, intervallando riposi pomeridiani. Nonostante queste premesse l’invecchiamento non può essere assunto a priori come la spiegazione dell’insonnia.
Infatti molti fattori possono compromettere il sonno nell’anziano: nicturia, sindromi dolorose, scompenso cardiaco, BPCO, Parkinson, sleep apnea (frequenza aumentata in età avanzata), rest leg syndrome , demenza, ansia o depressione.
Come nei giovani i trattamenti non farmacologici dovrebbero avere precedenza su qualsiasi altro tipo di terapia. In Accordo con le linee guida AASM del 2008 la terapia cognitivo comportamentale ha dimostrato efficacia anche in questa fascia di età, in particolare l’attività aerobica e l’igiene del sonno hanno dato ottimi risultati. Se necessario prescrivere una terapia farmacologica, gli ipnoinducenti dovrebbero essere usati sempre partendo da dosi ridotte, mai dalle dosi standard per gli adulti sani. I farmaci di questa categoria tendono ad avere un effetto a maggiore durata d’azione negli anziani a causa dei cambiamenti fisiopatologici nel metabolismo e nei processi di eliminazione dell’anziano. Dati epidemiologici ci dimostrano infatti come il tasso di fratture ed incidenti domestici notturni negli anziani sopposti a terapie di questo tipo (es. durante uso del bagno) risultino molto più alti rispetto a controlli non trattati con ipnoinducenti. Parimenti il prolungarsi anomalo degli effetti anche nelle ore diurne risulta molto a rischio di compromissione delle performance dell’anziano, comprese quelle di guida dei veicoli.
AUTORE
Daniele Angioni, Antonio Gabriele Bonagura
BIBLIOGRAFIA
Gabapentin e Pregabalin: hanno dimostrato di aumentare il sonno ad onde lente e l’efficienza del sonno CW Bazil.
Gabapentin Improves sleep in presence oh alcohol. J clin Sleep Med 2005I Hindmarch et. Al A double blind study in healthy volunteers to assess the effects on sleep of pregabalin xompared with alprazolam and placebo. Sleep 2005
Balfour JA, Figgitt DP. Telithromycin. Drugs 2001; 61: 815-829.Demolis JL, et al. Effect of telithromycin on ventricular repolarization in healthy subjects (abstract no. 651). 7th World Conference on Clinical Pharmacology and Therapeutics IUPHAR – Division of Clinical Pharmacology, and 4th Congress of the European Association for Clinical Pharmacology and Therapeutics: 2000 Jul 15-20: Florence, 168.F.
Rossi V. Cuomo C.Riccardi Farmacologia principi di base e applicazioni terapeutiche
L’American Academy of Sleep Medicine 25 e la National Institutes of Health 51 hanno pubblicato delle lineE guida per la diagnosi e la gestione dell’insonnia. John W. Winkelman , Insomnia Disorder, 2015 NEJMRN Hanzen et al Sedative hypnotic medication use and the risk of motor vehicle crash, AMJ public health 2015 JuneLowes, R. FDA OKs New Kind of Sleep Drug Suvorexant (Belsomra). Medscape Medical News. Available athttp://www.medscape.com/viewarticle/829893. Accessed: August 16, 2014.[Guideline] Schutte-Rodin S, Broch L, Buysse D, Dorsey C, Sateia M. Clinical guideline for the evaluation and management of chronic insomnia in adults. J Clin Sleep Med. 2008 Oct 15. 4(5):487-504. [Medline].
[Full Text].Montagna P, Gambetti P, Cortelli P, Lugaresi E. Familial and sporadic fatal insomnia. Lancet Neurol. 2003 Mar. 2(3):167-76. [Medline].Edinger JD, Means MK. Cognitive-behavioral therapy for primary insomnia. Clin Psychol Rev. 2005 Jul. 25(5):539-58. [Medline].
Chesson AL Jr, Anderson WM, Littner M, Davila D, Hartse K, Johnson S, et al. Practice parameters for the nonpharmacologic treatment of chronic insomnia. An American Academy of Sleep Medicine report. Standards of Practice Committee of the American Academy of Sleep Medicine. Sleep. 1999 Dec 15. 22(8):1128-33. [Medline].
Morgenthaler T, Kramer M, Alessi C, Friedman L, Boehlecke B, Brown T, et al. Practice parameters for the psychological and behavioral treatment of insomnia: an update. An american academy of sleep medicine report. Sleep. 2006 Nov 1. 29(11):1415-9. [Medline].
American Academy of Sleep Medicine. ICSD2 – International Classification of Sleep Disorders. Diagnostic and Coding Manual. 2nd. Westchester, Ill: American Academy of Sleep Medicine; 2005. 1-32.Buysse DJ. Diagnosis and Classification of Insomnia Disorders. In: Insomnia: Principles and Management. Szuba MP, Kloss JD, Dinges DF, Eds. Cambridge University Press, Cambridge UK, 2003, et al.Chokroverty S. Sleep Disorders Medicine: Basic Science, Technical Considerations, and Clinical Aspects, 3rd edition, p361. WB Saunders, Philadelphia, et al.The Gallup organization.
The Gallup study of sleeping habits. Princeton, NJ,: The Gallup Organization; 1979.American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders. Fifth. Arlington, VA: American Psychiatric Association; 2013.Edinger JD, Means MK, Carney CE, Krystal AD. Psychomotor performance deficits and their relation to prior nights’ sleep among individuals with primary insomnia. Sleep. 2008 May 1. 31(5):599-607. [Medline].
[Full Text].
Zammit GK, Weiner J, Damato N, Sillup GP, McMillan CA. Quality of life in people with insomnia. Sleep. 1999 May 1. 22 Suppl 2:S379-85. [Medline].
Daley M, Morin CM, LeBlanc M, Grégoire JP, Savard J. The economic burden of insomnia: direct and indirect costs for individuals with insomnia syndrome, insomnia symptoms, and good sleepers. Sleep. 2009 Jan 1. 32(1):55-64. [Medline].
[Full Text].National Institutes of Health State of the Science Conference statement on Manifestations and Management of Chronic Insomnia in Adults, June 13-15, 2005. Sleep. 2005 Sep 1. 28(9):1049-57.[Medline].
Smith MT, Huang MI, Manber R. Cognitive behavior therapy for chronic insomnia occurring within the context of medical and psychiatric disorders. Clin Psychol Rev. 2005 Jul. 25(5):559-92. [Medline].
Morin CM, Bootzin RR, Buysse DJ, Edinger JD, Espie CA, Lichstein KL. Psychological and behavioral treatment of insomnia:update of the recent evidence (1998-2004). Sleep. 2006 Nov 1. 29(11):1398414.[Medline].
Czeisler CA, Cajochen C, Turek FW. Melatonin in the regulation of sleep and circadian rhythms. Kryger MH, Roth T, Dement WC, eds. Principles and Practice of Sleep Medicine. New York: McGraw-Hill; 2000. 400-6.Saper CB, Scammell TE, Lu J. Hypothalamic regulation of sleep and circadian rhythms. Nature. 2005 Oct 27. 437(7063):1257-63. [Medline].
Saper CB, Chou TC, Scammell TE. The sleep switch: hypothalamic control of sleep and wakefulness.Trends Neurosci. 2001 Dec. 24(12):726-31. [Medline].Baumann CR, Bassetti CL. Hypocretins (orexins) and sleep-wake disorders. Lancet Neurol. 2005 Oct. 4(10):673-82. [Medline].Lu J, Greco MA. Sleep circuitry and the hypnotic mechanism of GABAA drugs. J Clin Sleep Med. 2006 Apr 15. 2(2):S19-26. [Medline].
Nutt D. GABAA receptors: subtypes, regional distribution, and function. J Clin Sleep Med. 2006 Apr 15. 2(2):S7-11. [Medline].
Krystal A. Pharmacological Treatment: Other Medications. Kryger MH, Roth T, Dement WC, eds. Principles and Practice of Sleep Medicine. 5th ed. St. Louis, Mo: Elsevier Saunders; 2010. 916-30.Drake CL and Roth T. Predisposition in the Evolution of Insomnia: Evidence, Potential Mechanisms, and Future Directions. Sleep Med Clin. 2006. 1(3):333-350.Nofzinger EA, Buysse DJ, Germain A, Price JC, Miewald JM, Kupfer DJ. Functional neuroimaging evidence for hyperarousal in insomnia. Am J Psychiatry. 2004 Nov. 161(11):2126-8. [Medline].
Bonnet MH, Arand DL. 24-Hour metabolic rate in insomniacs and matched normal sleepers. Sleep. 1995 Sep. 18(7):581-8. [Medline].
Bonnet MH, Arand DL. Caffeine use as a model of acute and chronic insomnia. Sleep. 1992 Dec. 15(6):526-36. [Medline].
Vgontzas AN, Bixler EO, Lin HM, Prolo P, Mastorakos G, Vela-Bueno A, et al. Chronic insomnia is associated with nyctohemeral activation of the hypothalamic-pituitary-adrenal axis: clinical implications. J Clin Endocrinol Metab. 2001 Aug. 86(8):3787-94. [Medline].
Lack LC, Gradisar M, Van Someren EJ, Wright HR, Lushington K. The relationship between insomnia and body temperatures. Sleep Med Rev. 2008 Aug. 12(4):307-17. [Medline].
Spielman AJ, Caruso LS, Glovinsky PB. A behavioral perspective on insomnia treatment. Psychiatr Clin North Am. 1987 Dec. 10(4):541-53. [Medline].
Crocker A, Sehgal A. Genetic analysis of sleep. Genes Dev. 2010 Jun 15. 24(12):1220-35. [Medline].
[Full Text].Rétey JV, Adam M, Khatami R, Luhmann UF, Jung HH, Berger W, et al. A genetic variation in the adenosine A2A receptor gene (ADORA2A) contributes to individual sensitivity to caffeine effects on sleep.Clin Pharmacol Ther. 2007 May. 81(5):692-8. [Medline].
Hamet P, Tremblay J. Genetics of the sleep-wake cycle and its disorders. Metabolism. 2006 Oct. 55(10 Suppl 2):S7-12. [Medline].
Buhr A, Bianchi MT, Baur R, Courtet P, Pignay V, Boulenger JP, et al. Functional characterization of the new human GABA(A) receptor mutation beta3(R192H). Hum Genet. 2002 Aug. 111(2):154-60. [Medline].
Montagna P, Cortelli P, Tinuper P, et al. Fatal familial insomnia. Guilleminault C, Montagna P, Lugaresi E, Gambetti P, editors. Fatal Familial Insomnia: Inherited Prion Disease, Sleep and the Thalamus. New York, NY: Raven Press; 1994. 1–14.Gambetti O, Medori P, Manetto V, et al. Fatal familial insomnia: S prion disease with distinctive histopathological and genotypic features. Guilleminault C, Montagna P, Lugaresi E, Gambetti P, editors.Fatal Familial Insomnia Inherited Prion Disease, Sleep and the Thalamus. New York, NY: Raven Press; 1994. 7–32.Montagna P, Cortelli P, Avoni P, Tinuper P, Plazzi G, Gallassi R, et al. Clinical features of fatal familial insomnia: phenotypic variability in relation to a polymorphism at codon 129 of the prion protein gene. Brain Pathol. 1998 Jul. 8(3):515-20. [Medline].
Goldfarb LG, Petersen RB, Tabaton M, Brown P, LeBlanc AC, Montagna P, et al. Fatal familial insomnia and familial Creutzfeldt-Jakob disease: disease phenotype determined by a DNA polymorphism. Science. 1992 Oct 30. 258(5083):806-8. [Medline].
Scaravilli F, Cordery RJ, Kretzschmar H, Gambetti P, Brink B, Fritz V, et al. Sporadic fatal insomnia: a case study. Ann Neurol. 2000 Oct. 48(4):665-8. [Medline].Morin CM, Rodrigue S, Ivers H. Role of stress, arousal, and coping skills in primary insomnia. Psychosom Med. 2003 Mar-Apr. 65(2):259-67. [Medline].Ford DE, Kamerow DB. Epidemiologic study of sleep disturbances and psychiatric disorders. An opportunity for prevention?. JAMA. 1989 Sep 15. 262(11):1479-84. [Medline].
Insomnia. American Academy of Sleep Medicine. The International Classification of Sleep Disorders. 2nd ed. Westchester, Illinois: American Academy of Sleep Medicine; 2005. 1-31.Taylor DJ, Mallory LJ, Lichstein KL, Durrence HH, Riedel BW, Bush AJ. Comorbidity of chronic insomnia with medical problems. Sleep. 2007 Feb 1. 30(2):213-8. [Medline].
Johnson EO, Roth T, Schultz L, Breslau N. Epidemiology of DSM-IV insomnia in adolescence: lifetime prevalence, chronicity, and an emergent gender difference. Pediatrics. 2006 Feb. 117(2):e247-56. [Medline].
Ohayon MM. Epidemiology of insomnia: what we know and what we still need to learn. Sleep Med Rev. 2002 Apr. 6(2):97-111. [Medline].
Morin CM, LeBlanc M, Daley M, Gregoire JP, Mérette C. Epidemiology of insomnia: prevalence, self-help treatments, consultations, and determinants of help-seeking behaviors. Sleep Med. 2006 Mar. 7(2):123-30.[Medline].
Calem M, Bisla J, Begum A, Dewey M, Bebbington PE, Brugha T, et al. Increased prevalence of insomnia and changes in hypnotics use in England over 15 years: analysis of the 1993, 2000, and 2007 National Psychiatric Morbidity Surveys. Sleep. 2012 Mar 1. 35(3):377-84. [Medline]. [Full Text].
Zhang B, Wing YK. Sex differences in insomnia: a meta-analysis. Sleep. 2006 Jan 1. 29(1):85-93.[Medline].
Kravitz HM, Ganz PA, Bromberger J, Powell LH, Sutton-Tyrrell K, Meyer PM. Sleep difficulty in women at midlife: a community survey of sleep and the menopausal transition. Menopause. 2003 Jan-Feb. 10(1):19-28. [Medline].
Strine TW, Chapman DP, Ahluwalia IB. Menstrual-related problems and psychological distress among women in the United States. J Womens Health (Larchmt). 2005 May. 14(4):316-23. [Medline].
Ruiter ME, DeCoster J, Jacobs L, Lichstein KL. Sleep disorders in African Americans and Caucasian Americans: a meta-analysis. Behav Sleep Med. 2010. 8(4):246-59. [Medline].
Monane M. Insomnia in the elderly. J Clin Psychiatry. 1992 Jun. 53 Suppl:23-8. [Medline].
Krystal AD. Treating the health, quality of life, and functional impairments in insomnia. J Clin Sleep Med. 2007 Feb 15. 3(1):63-72. [Medline].
Chien KL, Chen PC, Hsu HC, Su TC, Sung FC, Chen MF, et al. Habitual sleep duration and insomnia and the risk of cardiovascular events and all-cause death: report from a community-based cohort. Sleep. 2010 Feb 1. 33(2):177-84. [Medline]. [Full Text].
Phillips B, Buzková P, Enright P. Insomnia did not predict incident hypertension in older adults in the cardiovascular health study. Sleep. 2009 Jan 1. 32(1):65-72. [Medline]. [Full Text].
Gangwisch JE, Heymsfield SB, Boden-Albala B, Buijs RM, Kreier F, Pickering TG, et al. Short sleep duration as a risk factor for hypertension: analyses of the first National Health and Nutrition Examination Survey. Hypertension. 2006 May. 47(5):833-9. [Medline].
Gottlieb DJ, Redline S, Nieto FJ, Baldwin CM, Newman AB, Resnick HE, et al. Association of usual sleep duration with hypertension: the Sleep Heart Health Study. Sleep. 2006 Aug 1. 29(8):1009-14. [Medline].
Vgontzas AN, Liao D, Bixler EO, Chrousos GP, Vela-Bueno A. Insomnia with objective short sleep duration is associated with a high risk for hypertension. Sleep. 2009 Apr 1. 32(4):491-7. [Medline]. [Full Text].
Lanfranchi PA, Pennestri MH, Fradette L, Dumont M, Morin CM, Montplaisir J. Nighttime blood pressurein normotensive subjects with chronic insomnia: implications for cardiovascular risk. Sleep. 2009 Jun 1. 32(6):760-6. [Medline]. [Full Text].
Knutson KL, Van Cauter E, Rathouz PJ, Yan LL, Hulley SB, Liu K, et al. Association between sleep and blood pressure in midlife: the CARDIA sleep study. Arch Intern Med. 2009 Jun 8. 169(11):1055-61.[Medline].
[Full Text].Baglioni C, Battagliese G, Feige B, Spiegelhalder K, Nissen C, Voderholzer U, et al. Insomnia as a predictor of depression: a meta-analytic evaluation of longitudinal epidemiological studies. J Affect Disord. 2011 Dec. 135(1-3):10-9. [Medline].
Ohayon MM, Roth T. Place of chronic insomnia in the course of depressive and anxiety disorders. J Psychiatr Res. 2003 Jan-Feb. 37(1):9-15. [Medline].
Chesson A Jr, Hartse K, Anderson WM, Davila D, Johnson S, Littner M, et al. Practice parameters for the evaluation of chronic insomnia. An American Academy of Sleep Medicine report. Standards of Practice Committee of the American Academy of Sleep Medicine. Sleep. 2000 Mar 15. 23(2):237-41. [Medline].
Natale V, Plazzi G, Martoni M. Actigraphy in the assessment of insomnia: a quantitative approach. Sleep. 2009 Jun 1. 32(6):767-71. [Medline].
[Full Text].Morin CM, Hauri PJ, Espie CA, Spielman AJ, Buysse DJ, Bootzin RR. Nonpharmacologic treatment of chronic insomnia. An American Academy of Sleep Medicine review. Sleep. 1999 Dec 15. 22(8):1134-56.[Medline].
Jacobs GD, Pace-Schott EF, Stickgold R, Otto MW. Cognitive behavior therapy and pharmacotherapy for insomnia: a randomized controlled trial and direct comparison. Arch Intern Med. 2004 Sep 27. 164(17):1888-96. [Medline].
Irwin MR, Cole JC, Nicassio PM. Comparative meta-analysis of behavioral interventions for insomnia and their efficacy in middle-aged adults and in older adults 55+ years of age. Health Psychol. 2006 Jan. 25(1):3-14. [Medline].
Manber R, Edinger JD, Gress JL, San Pedro-Salcedo MG, Kuo TF, Kalista T. Cognitive behavioral therapy for insomnia enhances depression outcome in patients with comorbid major depressive disorder and insomnia. Sleep. 2008 Apr 1. 31(4):489-95. [Medline]. [Full Text].
Edinger JD, Wohlgemuth WK, Radtke RA, Coffman CJ, Carney CE. Dose-response effects of cognitive-behavioral insomnia therapy: a randomized clinical trial. Sleep. 2007 Feb 1. 30(2):203-12. [Medline].
Buysse DJ, Germain A, Moul DE, et al. Efficacy of brief behavioral treatment for chronic insomnia in older adults. Arch Intern Med. 2011 May 23. 171(10):887-95. [Medline]. [Full Text].
Morin CM, Beaulieu-Bonneau S, LeBlanc M, Savard J. Self-help treatment for insomnia: a randomized controlled trial. Sleep. 2005 Oct 1. 28(10):1319-27. [Medline].
Sivertsen B, Omvik S, Pallesen S, Bjorvatn B, Havik OE, Kvale G, et al. Cognitive behavioral therapy vs zopiclone for treatment of chronic primary insomnia in older adults: a randomized controlled trial. JAMA. 2006 Jun 28. 295(24):2851-8. [Medline].
Morin CM, Vallieres A, Guay B, Ivers H, Savard J, Merette C, et al. Cognitive behavioral therapy, singly and combined with medication, for persistent insomnia. JAMA. May 20 2009. 301(19):2005-15.Krystal AD, Walsh JK, Laska E, Caron J, Amato DA, Wessel TC, et al. Sustained efficacy of eszopiclone over 6 months of nightly treatment: results of a randomized, double-blind, placebo-controlled study in adults with chronic insomnia. Sleep. 2003 Nov 1. 26(7):793-9. [Medline].
Walsh JK, Krystal AD, Amato DA, Rubens R, Caron J, Wessel TC, et al. Nightly treatment of primary insomnia with eszopiclone for six months: effect on sleep, quality of life, and work limitations. Sleep. 2007 Aug 1. 30(8):959-68. [Medline].
Roth T, Walsh JK, Krystal A, Wessel T, Roehrs TA. An evaluation of the efficacy and safety of eszopiclone over 12 months in patients with chronic primary insomnia. Sleep Med. 2005 Nov. 6(6):487-95. [Medline].
Krystal AD, Erman M, Zammit GK, Soubrane C, Roth T. Long-term efficacy and safety of zolpidem extended-release 12.5 mg, administered 3 to 7 nights per week for 24 weeks, in patients with chronic primary insomnia: a 6-month, randomized, double-blind, placebo-controlled, parallel-group, multicenter study. Sleep. 2008 Jan 1. 31(1):79-90. [Medline].
[Full Text].Jeffrey S. FDA recommends lower bedtime dose for zolpidem. Medscape Medical News. Jan 10, 2013. Available at http://www.medscape.com/viewarticle/777431. Accessed: Jan 16, 2013.FDA Drug Safety Communication: Risk of next-morning impairment after use of insomnia drugs; FDA requires lower recommended doses for certain drugs containing zolpidem (Ambien, Ambien CR, Edluar, and ZolpiMist). US Food and Drug Administration. Available athttp://www.fda.gov/Drugs/DrugSafety/ucm334033.htm. Accessed: January 10, 2013.Jeffrey S. FDA label changes for zolpidem products. Medcape Medical News. May 14, 2013. [Full Text].Morgenthaler TI, Silber MH. Amnestic sleep-related eating disorder associated with zolpidem. Sleep Med. 2002 Jul. 3(4):323-7. [Medline].
Chiang A, Krystal A. Report of two cases where sleep related eating behavior occurred with the extended-release formulation but not the immediate-release formulation of a sedative-hypnotic agent. J Clin Sleep Med. 2008 Apr 15. 4(2):155-6. [Medline]. [Full Text].
Roehrs TA, Randall S, Harris E, Maan R, Roth T. Twelve months of nightly zolpidem does not lead to dose escalation: a prospective placebo-controlled study. Sleep. 2011 Feb 1. 34(2):207-12. [Medline]. [Full Text].
Zammit G, Erman M, Wang-Weigand S, Sainati S, Zhang J, Roth T. Evaluation of the efficacy and safety of ramelteon in subjects with chronic insomnia. J Clin Sleep Med. 2007 Aug 15. 3(5):495-504. [Medline].
[Full Text].Zammit G, Wang-Weigand S, Rosenthal M, Peng X. Effect of ramelteon on middle-of-the-night balance in older adults with chronic insomnia. J Clin Sleep Med. 2009 Feb 15. 5(1):34-40. [Medline].
[Full Text].Mayer G, Wang-Weigand S, Roth-Schechter B, Lehmann R, Staner C, Partinen M. Efficacy and safety of 6-month nightly ramelteon administration in adults with chronic primary insomnia. Sleep. 2009 Mar 1. 32(3):351-60. [Medline].
[Full Text].Roth T, Heith Durrence H, Jochelson P, Peterson G, Ludington E, Rogowski R, et al. Efficacy and safety of doxepin 6 mg in a model of transient insomnia. Sleep Med. 2010 Oct. 11(9):843-7. [Medline].
Krystal AD, Durrence HH, Scharf M, Jochelson P, Rogowski R, Ludington E, et al. Efficacy and Safety of Doxepin 1 mg and 3 mg in a 12-week Sleep Laboratory and Outpatient Trial of Elderly Subjects with Chronic Primary Insomnia. Sleep. 2010 Nov. 33(11):1553-61. [Medline]. [Full Text].
Zhang D, Tashiro M, Shibuya K, et al. Next-day residual sedative effect after nighttime administration of an over-the-counter antihistamine sleep aid, diphenhydramine, measured by positron emission tomography. J Clin Psychopharmacol. 2010 Dec;30(6):694… Zhang D, Tashiro M, Shibuya K, et al. Next-day residual sedative effect after nighttime administration of an over-the-counter antihistamine sleep aid, diphenhydramine, measured by positron emission tomography. J Clin Psychopharmacol. 2010 Dec;30(6):694-701.Brzezinski A, Vangel MG, Wurtman RJ, Norrie G, Zhdanova I, Ben-Shushan A, et al. Effects of exogenous melatonin on sleep: a meta-analysis. Sleep Med Rev. 2005 Feb. 9(1):41-50. [Medline].
Buscemi N, Vandermeer B, Hooton N, Pandya R, Tjosvold L, Hartling L, et al. Efficacy and safety of exogenous melatonin for secondary sleep disorders and sleep disorders accompanying sleep restriction: meta-analysis. BMJ. 2006 Feb 18. 332(7538):385-93. [Medline].
Wade AG, Ford I, Crawford G, et al. Nightly treatment of primary insomnia with prolonged release melatonin for 6 months: a randomized placebo controlled trial on age and endogenous melatonin as predictors of efficacy and safety. BMC Med. 2010 Aug 16;8… Wade AG, Ford I, Crawford G, et al. Nightly treatment of primary insomnia with prolonged release melatonin for 6 months: a randomized placebo controlled trial on age and endogenous melatonin as predictors of efficacy and safety. BMC Med. 2010 Aug 16;8:51. Full text: http://www.biomedcentral.com/1741-7015/8/51.Rondanelli M, Opizzi A, Monteferrario F, Antoniello N, Manni R, Klersy C. The effect of melatonin, magnesium, and zinc on primary insomnia in long-term care facility residents in Italy: a double-blind, placebo-controlled clinical trial. J Am Geriatr Soc. 2011 Jan. 59(1):82-90. [Medline].
Bent S, Padula A, Moore D. Valerian for sleep: a systematic review and meta-analysis. Am J Med. Dec 2006. 119(12):1005-12.Fernández-San-Martín MI, Masa-Font R, Palacios-Soler L, Sancho-Gómez P, Calbó-Caldentey C, Flores-Mateo G. Effectiveness of Valerian on insomnia: a meta-analysis of randomized placebo-controlled trials.Sleep Med. 2010 Jun. 11(6):505-11. [Medline].
Taavoni S, Ekbatani N, Kashaniyan M, Haghani H. Effect of valerian on sleep quality in postmenopausal women: a randomized placebo-controlled clinical trial. Menopause. 2011 Sep. 18(9):951-5. [Medline].
Meolie AL, Rosen C, Kristo D, Kohrman M, Gooneratne N, Aguillard RN, et al. Oral nonprescription treatment for insomnia: an evaluation of products with limited evidence. J Clin Sleep Med. 2005 Apr 15. 1(2):173-87. [Medline].
Sun JL, Sung MS, Huang MY, Cheng GC, Lin CC. Effectiveness of acupressure for residents of long-term care facilities with insomnia: a randomized controlled trial. Int J Nurs Stud. 2010 Jul. 47(7):798-805.[Medline].
Ancoli-Israel S, Martin JL. Insomnia and daytime napping in older adults. J Clin Sleep Med. 2006 Jul 15. 2(3):333-42. [Medline].
Kryger M, Monjan A, Bliwise D, Ancoli-Israel S. Sleep, health, and aging. Bridging the gap between science and clinical practice. Geriatrics. 2004 Jan. 59(1):24-6, 29-30. [Medline].
Liu L and Ancoli-Israel S. Insomnia in the Older Adult. Sleep Med Clin. 2006. 1(3):409-422.Reid KJ, Baron KG, Lu B, Naylor E, Wolfe L, Zee PC. Aerobic exercise improves self-reported sleep and quality of life in older adults with insomnia. Sleep Med. 2010 Oct. 11(9):934-40. [Medline]. [Full Text].
Brooks M. FDA Cuts Starting Dose of Eszopiclone (Lunesta) in Half. Medscape Medical News. May 15 2014. [Full Text].








