Fin dalla loro scoperta negli anni ’40 i corticosteroidi sono diventati uno tra i farmaci più usati ed efficaci nel trattamento di patologie infiammatorie ed autoimmuni. Usati anche come supplemento nell’insufficienza surrenalica così come nella gestione di disturbi dermatologici, polmonari, reumatologici, oftalmici, ematologici e gastrointestinali hanno cambiato radicalmente la storia clinica di alcune patologie.
USI CLINICI CORTICOSTEROIDI: LINK
Il cortisolo, principale glucocorticoide naturale, è provvisto sia di effetti sul metabolismo glicidico ed elettrolitico sia di attività antinfiammatoria, ed è il termine di paragone per l’attività dei glucocorticoidi sintetici. Le modificazioni chimiche sulla molecola del cortisolo hanno prodotto composti di sintesi con elevata attività antinfiammatoria e trascurabile azione mineralcorticoide. D’altra parte non è ancora stato possibile separare l’azione antinfiammatoria dagli effetti sul metabolismo dei carboidrati, lipidi e proteine, (responsabile dei principali effetti avversi) probabilmente perchè mediati dallo stesso recettore.
Ne conviene quindi come i glucocorticoidi di sintesi più potenti come antinfiammatori saranno anche quelli che causano maggiori reazioni avverse metaboliche.
Prima di analizzare le caratteristiche di questi farmaci però definiamo cosa si intende per attività glucocorticoide e mineralcorticoide:
L’ attività mineralcorticoide riveste un ruolo importante nella regolazione della funzione renale.I mineralcorticoidi esercitano la loro azione sul trasporto di ioni nelle cellule epiteliali dei tubuli renali e sono primariamente coinvolti nella regolazione del bilancio idroelettrolitico.
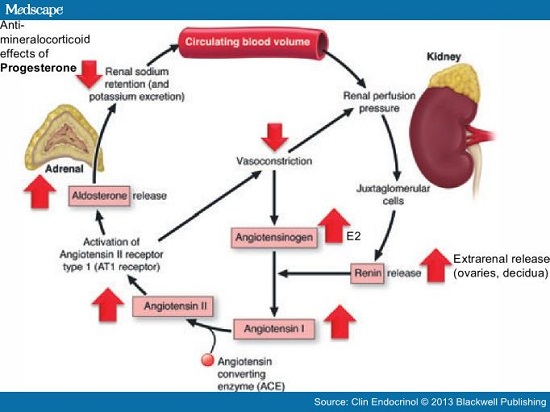
I glucocorticoidi invece, come già anticipato, coinvolgono in modo predominante il metabolismo di carboidrati, grassi e proteine, ed hanno azione antinfiammatoria, immunosopprressiva, antiproliferativa e vasocostrittrice.
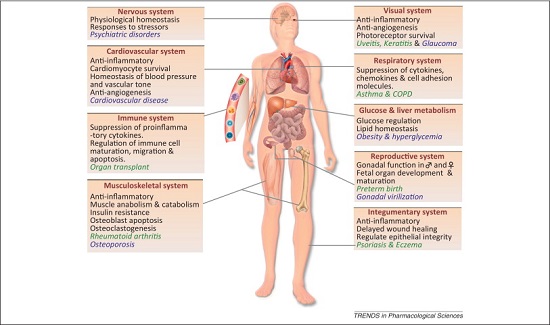
NB: in questo articolo si farà particolare riferimento ai cortisonici di sintesi somministrabili per os ma anche i.m. ed e.v. Le formulazioni topiche verranno trattate separatamente.
FARMACOCINETICA
Tra i parametri fondamentali da prendere in considerazione in caso di somministrazione di glucocorticoidi vi sono: attività antinfiammatoria, attività mineralcorticoide, durata d’azione del farmaco, picco di concentrazione plasmatica.
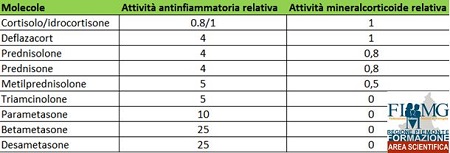
Attività antinfiammatoria
- Molecola con maggiore attività antinfiammatoria: Desametasone, Betametasone
- Molecola con minore attività antinfiammatoria: Idrocortisone
Attività Mineralcorticoide
- Molecola con maggiore attività mineralcorticoide: Idrocortisone
- Molecola con minore attività mineralcorticoide: Metilprednisolone
- Molecola con attività mineralcorticoide nulla o trascurabile: Betametasone/Desametasone
Durata d’azione
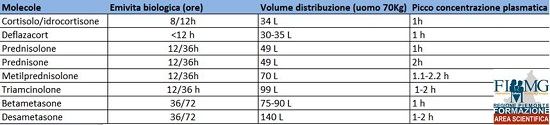
La durata d’azione può essere approssimata per semplicità tramite l’analisi dell’emivita biologica.
- Molecola con maggiore emivita: Desametasone/Betametasone ( 1-3 giorni)
- Molecola con minore emivita: Idrocortisone (8-12h)
Altri parametri farmacocinetici
Tra i parametri considerati nella tabella vi è anche il volume di distribuzione che tuttavia correla positivamente con l’emivita plasmatica e biologica*** del farmaco, secondo la formula :T ½= (0,693x Vd)/CL
Dove T ½ = emivita plasmatica; Vd= volume di distribuzione (capacità di diffusione e penetrazione dei farmaci nei vari tessuti e organi); CL= clearance plasmatica (volume di plasma depurato dal farmaco per unità di tempo)
L’emivita quindi tende a variare in modo direttamente proporzionale al suo volume di distribuzione ed in modo inversamente proporzionale alla sua CL. Il Vd rappresenta anche, in linea teorica, la capacità di superare,la barriera ematoencefalica (prgressivamente per Vd > 16L). Più è alto il volume di distribuzione, più è prolungata l’esposizione al farmaco (emivita e durata del trattamento) maggiore sarà la capacità di raggiungere la circolazione ipotalamica ed ipofisaria; in questo modo può essere esercitata una attività di feedback negativo sul sistema ipotalamico-ipofisario-surrenale tramite la soppressione ipotalamica di produzione di CRH e il conseguente ridotto rilascio di ACTH da parte dell’ipofisi.
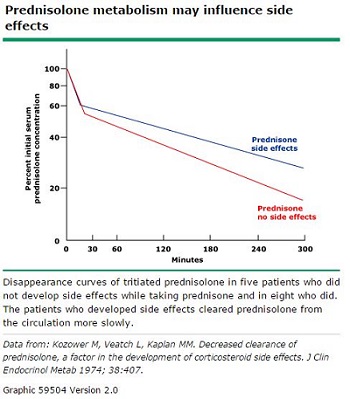
Il grafico che segue rappresenta il metabolismo del prednisolone in soggetti con clearance ritardata del farmaco Vs soggetti noramli e l’aumento conseguente di eventi avversi nel primo gruppo; al di là del singolo esempio il grafico mette in luce come l’insorgenza di tossicità sia estremamente legata alla durata prolungata di concentrazione elevate nel siero.
Il picco di concentrazione plasmatica invece ci fornisce una discreta approssimazione sulla rapidità d’azione del farmaco. In questo caso è molto simile in tutti i tipi di glucocorticoidi somministrati per Os, ovvero circa 2 ore.
Ulteriori variazioni sono legate al tipo di somministrazione ed in questo caso valgono le regole generali per le quali:
Somminstrazione orale: semplice, sicura, economica, buona compliance MA non adatta a situazioni di emergenza, soggetta ad effetto di primo passaggio ed interazioni con alimenti
Somministrazione sottocute: rapidità di assorbimento maggiore rispetto alla via orale
Somministrazione intramuscolo: rapidità di assorbimento maggiore rispetto alla via orale e sottocutanea
Somministrazione endovena: effetto immediato nell’ordine di secondi/minuti soprattutto se a bolo, effetto del farmaco modulabile per le infusioni continue
NB: via sublinguale ha rapida insorgenza grazie a via circolatoria privilegiata ed assenza effetto di primo passaggio MA incertezza del dosaggio!
***ATTENZIONE: in precedenza si è parlato di emivita biologica (come espresso in tabella) non è sinonimo di emivita plasmatica. La prima rappresenta infatti la durata dell’effetto biologico complessivo e in linea generale correla con l’emivita plasmatica che tuttavia rappresenta il parametro farmacocinetico che indica il tempo necessario affinchè la concentrazione plasmatica di un farmaco si dimezzi (ovvero si riduca del 50%).
DOSI EQUIVALENTI DI CORTICOSTEROIDI
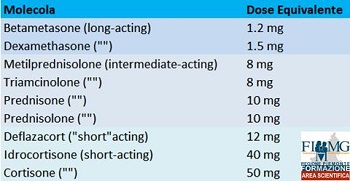
Si consigliano due utili applicazioni per smartphone gratuite per la conversione dei corticosteroidi:
Android: Steroid converter
Apple: Corticonverter

TAPERING
Nonostante sia uso comune in medicina generale “scalare” la dose di corticosteroidi anche dopo brevi periodi di trattamento la letteratura ci dice come non sia necessaria nessuna riduzione di dose graduale se la terapia con i cortisonici è uguale o inferiore a 3 settimane, anche a dosaggi elevati. In questi casi il trattamento può essere interrotto direttamente.
Quindi l’asse ipotalamo-ipofisi-surrene va considerato fino a prova contraria:
NON SOPPRESSO (non “scalare”):
- per somministrazioni di glucocorticoidi a qualsiasi dose per somministrazioni non parenterali per meno di 3 settimane
- pazienti trattati con glucocorticoidi a giorni alterni a dosi fisiologiche
SOPPRESSO (“scalare”):
- chiunque abbia ricevuto più di 20mg di prednisone al giorno (o dose equivalente) per più di 3 settimane
- tutti i pazienti con segni clinici di Sindrome di Cushing
NB: in soggetti fragili o gravemente malati, il processo di tapering può comunque essere una buona scelta anche per terapie brevi al fine di non turbare fini equilibri clinici.
Obiettivo della riduzione di dose graduale è recuperare una normale responsività dell’asse IIS (ipotalamo-ipofisi-surrene) alla secrezione di corticosteroidi endogeni. Nella gran parte dei pazienti la secrezione di cortisolo endogena corrisponde a 5/7.5 mg di prednisone.
Esistono diversi schemi per la riduzione di dose delle terapie cortisoniche, in questa revisione verrà proposta quella presentata su UptoDate (Glucocorticoids Withdrawal) aggiornato al Novembre 2015.
REGOLA GENERALE: si consiglia un decremento ogni 1-2 settimane del 5-10% massimo 20% in base alla risposta del paziente, dilazionabili fino a 4 settimane nei soggetti più fragili.
Come scalare il cortisone?
- Ridurre la dose giornaliera di 5/10 mg ogni 1 o 2 settimane se la dose iniziale è superiore a 40 mg /die di prednisone o equivalente.
- Ridurre la dose giornaliera di 5 mg ogni 1 o 2 settimane se la dose iniziale è compresa tra 40 mg /die e 20 mg/die di prednisone o equivalente.
- Ridurre la dose giornaliera di 2,5 mg ogni 1 o 2 settimane se la dose iniziale è compresa tra 20 mg /die e 10 mg/die di prednisone o equivalente.
- Ridurre la dose giornaliera di 0,5 mg ogni 1 o 2 settimane se la dose iniziale è uguale o inferiore a 5 mg/die di prednisone o equivalente.
INTERAZIONE TRA CORTICOSTEROIDI E ALTRI FARMACI
Diversi farmaci possono interagire con i corticosteroidi come ad esempio gli antiacidi, tuttavia in particolar modo il principale meccanismo di azione che influenza la l’escrezione del farmaco è l’induzione o inibizione del Citocromo 3A. Di seguito si riportano le principali alterazioni
LINK INTERAZIONI CORTICOSTEROIDI (Per il corretto funzionamento del link, cliccare sull’indirizzo o copiare ed incollare sul proprio browser)
IN SINTESI: Glucocorticoidi quando e perchè?
Prednisone
Il prednisone è forse uno dei corticosteroidi sistemici più utilizzati. La sua attività glucocorticoide medio/alta, l’emivita intermedia e la sua discreta attività mineralcorticoide lo rendono uno dei farmaci verosimilmente più versatili e con gli effetti avversi più gestibili di questa classe, permettendo somministrazioni giornaliere (anche ripetute) tenendo conto della variabilità del fabbisogno corticosteroideo circardiano del malato e della patologia in trattamento. Circa l’80% di prednisone viene convertito a prednisolone, che ne rappresenta il metabolita attivo, grazie al metabolismo di primo passaggio epatico.
Prednisolone
Il prednisolone è quindi del tutto simile al prednisone con la differenza che non essendo sottoposto a effetto di primo passaggio ha una rapidità d’azione leggermente superiore e potrebbe essere usato efficacemente in soggetti affetti da patologie epatiche che quindi non riuscirebbero a convertire il prednisone in prednisolone.
Metilprednisolone
Il metilprednisolone invece, nonostante sia molto simile a prednisone e prednisolone (durata d’azione analoga) ha attività antinfiammatoria leggermente superiore e minori effetti mineralcorticoidi; potrebbe quindi essere preferito quando si vuole minimizzare la ritenzione idrica pur mantendendo i vantaggi farmacocinetici del prednisone.
Deflazacort
Poco utilizzato e poco conosciuto, il Deflazacort è un corticosteroide con relativa breve emivita il cui principale vantaggio è una nominale parziale dissociazione tra effetti antinfiammatori ed effetti sul metabolismo glucidico e del calcio; la tendenza sarebbe quindi quella di contenere l’aumento dei livelli di glucosio sierico e di calcemia. Il Deflazacort sarebbe ritenuto secondo alcuni studi il più adatto quando fosse necessario un glucocorticoide nei soggetti diabetici.
Desametasone/Betametasone
Il Desametasone invece come visto, ha attività mineralcorticoide quasi irrilevante, cosi come il Betametasone, ma è molto più potente rispetto agli altri farmaci steroidei ed ha durata d’azione decisamente più lunga rispetto a prednisone e prednisolone. D’altra parte, poiché l’aumento della potenza antinfiammatoria si accompagna ad un aumento della tossicità, l’indice terapeutico ***** di desametasone e betametasone non è migliore di quello, per esempio del Prednisolone. Vista la loro alta attività antinfiammatora sono più soggetti ad effetti avversi in particolare se il trattamento è protratto per lungo tempo. Per questi motivi andrebbero utilizzati solo per brevi periodi e in condizioni acute/severe.
*****INDICE TERAPEUTICO= DL50(dose letale)/DE50(dose efficace). Semplificando all’estremo il concetto più l’indice terapeutico è basso, più il farmaco è pericoloso, più l’indice terapeutico è alto più il farmaco è sicuro. Ne consegue che un farmaco con efficacia già presente a bassi dosaggi (dose efficace bassa) e estremamente tossico ad alti dosaggi (dose letale alta) avrà un profilo di sicurezza ottimo.
Cortisolo/Idrocortisone
Cortisolo e Idrocortisone hanno bassa potenza glucocorticoide. Vista però la loro importante azione mineralcorticoide, breve emivita e rapidità di azione possono essere usati per pazienti con insufficienza surrenalica o in particolari situazioni di emergenza. All’estremo opposto abbiamo il Fluridrocortisone con attività glucocorticoide 10 volte maggiore rispetto al cortisolo ma attività mineralcorticoide 125 volte maggiore rispetto al cortisolo, comunemente usato per rimpiazzare l’aldosterone nella malattia di Addison.
CURIOSITA’
Esistono formulazioni a rilascio modificato per alcuni glucocorticoidi che permettono monosomministrazioni giornaliere bypassando il problema di un’emivita troppo breve rispetto alle necessità terapeutiche. Questo è particolarmente utile per gli steroidi con media attività antinfiammatoria come il prednisone dove ad un minor rischio di effetti avversi si associerebbe una maggiore durata d’azione a picco di concentrazione plasmatica controllata. Nota negativa è che in Italia sono sovente registrati con indicazioni terapeutiche molto ristrette (es. artrite reumatoide) che rendono l’impiego di questi farmaci Off Label per qualsiasi altro utilizzo medico al di fuori di quello indicato.
AUTORE
Daniele Angioni
Un ringraziamento speciale alla Dott.ssa F. D’Agostino per la gentile concessione della letteratura proveniente da UpToDate
BIBLIOGRAFIA
Pharmacologic use of glucocorticoids; UptoDate; Lynnette K nieman, Andrè Lacroix, Kathryn A Martin (03/12/2015)
Glucocorticoid Withdrawal; UptoDate; Daniel E Furst Kenneth G Saag (03/12/2015)
F. Rossi V.Cuomo Farmacologia principi di base e applicazioni terapeutiche
Goodman & Gilman; Le basi farmacologiche della terapia, XII ed, Laurenze L. Brunton, Bruce A. Chabner, Björn C. Knollmann
Textbook of Pediatric Rheumatology Petty Laxer Lindsley Wedderbur 7th Edition Elsevier
Mager DE, Lin SX, Blum RA, Lates CD, Jusko WJ. Dose equivalency evaluation of major corticosteroids: pharmacokinetics and cell trafficking and cortisol dynamics. J Clin Pharmacol. 2003 Nov. 43(11):1216-27.[Medline].
Webb R, Singer M. Oxford Handbook of Critical Care. Oxford University Press. 2005.Kirwan JR. Systemic corticosteroids in rheumatology. In: Rheumatology, Hochberg MC, Silman AJ, Smolen JS (Eds), Mosby, St. Louis 2003. p.385. 2. Francisco GE, Honigberg IL, Stewart JT, et al. In vitro and in vivo bioequivalence of commercial prednisone tablets. Biopharm Drug Dispos 1984; 5:335.
Garg DC, Wagner JG, Sakmar E, et al. Rectal and oral absorption of methylprednisolone acetate. Clin Pharmacol Ther 1979; 26:232. 4.
Rose JQ, Yurchak AM, Jusko WJ, Powell D. Bioavailability and disposition of prednisone and prednisolone from prednisone tablets. Biopharm Drug Dispos 1980; 1:247. 5.
Legler UF, Benet LZ. Marked alterations in dose¬dependent prednisolone kinetics in women taking oral contraceptives. Clin Pharmacol Ther 1986; 39:425. 6.
Toothaker RD, Craig WA, Welling PG. Effect of dose size on the pharmacokinetics of oral hydrocortisone suspension. J Pharm Sci 1982; 71:1182. 7.
Pickup ME, Lowe JR, Leatham PA, et al. Dose dependent pharmacokinetics of prednisolone. Eur J Clin Pharmacol 1977; 12:213. 8.
Hill MR, Szefler SJ, Ball BD, et al. Monitoring glucocorticoid therapy: a pharmacokinetic approach. Clin Pharmacol Ther 1990; 48:390. 9.
Tornatore KM, Logue G, Venuto RC, Davis PJ. Pharmacokinetics of methylprednisolone in elderly and young healthy males. J Am Geriatr Soc 1994; 42:1118. 10.
Tornatore KM, Biocevich DM, Reed K, et al. Methylprednisolone pharmacokinetics, cortisol response, and adverse effects in black and white renal transplant recipients. Transplantation 1995; 59:729. 11.
Kimball CP. Psychological dependency on steroids? Ann Intern Med 1971; 75:111. 12.
Dixon RB, Christy NP. On the various forms of corticosteroid withdrawal syndrome. Am J Med 1980; 68:224. 13.
Richter B, Neises G, Clar C. Glucocorticoid withdrawal schemes in chronic medical disorders. A systematic review. Endocrinol Metab Clin North Am 2002; 31:751. 14.
Brignola C, De Simone G, Belloli C, et al. Steroid treatment in active Crohn’s disease: a comparison between two regimens of different duration. Aliment Pharmacol Ther 1994; 8:465. 15.
Hings IM, Filipovich AH, Miller WJ, et al. Prednisone therapy for acute graft¬versus¬host disease: shortversus long¬term treatment. A prospective randomized trial. Transplantation 1993; 56:577. 16.
Ueda N, Chihara M, Kawaguchi S, et al. Intermittent versus long¬term tapering prednisolone for initial therapy in children with idiopathic nephrotic syndrome. J Pediatr 1988; 112:122. 17.
Byyny RL. Withdrawal from glucocorticoid therapy. N Engl J Med 1976; 295:30. 18. Nelson AM, Conn DL. Series on pharmacology in practice. 9. Glucocorticoids in rheumatic disease. Mayo Clin Proc 1980; 55:758.
Family practice notebook at link http://www.fpnotebook.com/endo/pharm/systmccrtcstrd.htm
A different look at Corticosteroids, America Family Physician, Roger J. Zoorob. Dawn Cender
A practical guide to the monitoring and management of the complications of systemic ccorticosteroid therapy. Dora Lin, Alexandra Ahmet, Leanne Ward, Preetha Krishnamoorthy, Efrem D Mandelcorn, Richard Leigh, Jacques P Brown, Albert Cohen, Hardol Kim
Deflazacort versus other glucocorticoids: a comparison. Surajit Navak, Basanti Achariva
Comparison of two glucocorticoid preparations (deflazacort and prednisone) in the treatment of immune-mediated diseases. M. Scudeletti, F. Puppo, L. Lanza, L. Mantovani, O. Bosco, A. Iudice, B. Imbimbi, F. Indiveri