Come ogni anno, il 28 luglio si è celebrata la giornata mondiale contro l’epatite, promossa dall’OMS allo scopo di sensibilizzare sul tema delle epatiti virali e sulla loro prevenzione. Tale giorno è stato scelto in quanto ricorre la data di nascita di Baruch Samuel Blumberg, vincitore del premio Nobel per la Medicina del 1976 per avere identificato il virus dell’epatite B ed avere contribuito allo sviluppo del vaccino.
Il tema scelto quest’anno è “l’epatite non può aspettare”.
Non può aspettare perché:
- Ogni 30 secondi muore una persona per una malattia correlata all’epatite, anche nell’attuale crisi legata al COVID-19.
- Milioni di persone convivono con epatiti virali (e non solo) senza saperlo e non possono avere libero e pronto accesso ai test diagnostici.
- Molti pazienti che convivono con l’epatite sono ancora in attesa di avere accesso alle terapie salvavita.
- In tante zone del mondo i programmi di screening per le future madri ed i programmi di prevenzione vaccinale per i neonati non sono ancora sviluppati e solo il 42% dei nuovi nati nel mondo ha accesso alle vaccinazioni.
- I pazienti affetti da epatite sono ancora vittime di discriminazioni.
L’Organizzazione Mondiale della Sanità chiede ai Governi di tutti i Paesi uno sforzo congiunto per eliminare questa minaccia per la salute entro il 2030.
Le epatiti virali sono patologie infettive a carico del fegato. Ad oggi sono noti 5 virus epatici maggiori responsabili di tale infezione.
Altri virus possono poi causare quadri di epatite di gravità variabile e vengono definiti virus epatici minori: Citomegalovirus, virus di Epstein-Barr, virus Coxsackie ed Herpesvirus.
In circa il 10-20% dei casi l’agente eziologico risulta non noto.
L’intento di questo articolo è quello di approfondire le ultime novità sull’epidemiologia e sulla gestione (nella Medicina Generale, ma non solo) delle epatiti virali determinate dai virus epatici maggiori:
- HAV
- HBV
- HCV
- HDV
- HEV
HAV
Nel 2016 HAV ha causato 7134 decessi a livello mondiale.
HAV causa l’epatite dopo un periodo di incubazione di 15-50 giorni con un decorso generalmente autolimitante e benigno; sono frequenti anche le forme asintomatiche, specialmente in età pediatrica e nel corso di epidemie (l’ultima in Italia solo nel biennio 2016-2017).
Possono a volte verificarsi forme più gravi e con decorso protratto, fino a forme fulminanti, rapidamente fatali. La mortalità si attesta intorno al 0,1-0,3% (ma può arrivare fino all’1,8% negli adulti sopra i 50 anni.
L’epatite A non cronicizza: non esiste lo stato di portatore di HAV, né nel sangue, né nelle feci.
La trasmissione avviene per via oro-fecale. Il virus è presente nelle feci 7-10 giorni prima dell’esordio dei sintomi e fino a una settimana dopo, mentre è presente nel sangue solo per pochi giorni.
Il contagio avviene per contatto diretto da persona a persona o attraverso il consumo di acqua o di alcuni cibi crudi (o non cotti a sufficienza), soprattutto molluschi, allevati in acque contaminate da scarichi fognari contenenti il virus.
Come accennato in precedenza, nel biennio 2016-2017 è stata osservata un’importante epidemia di Epatite A in Europa e specialmente in Italia:
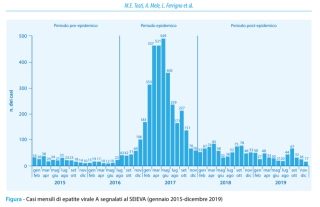
Dagli studi dell’Istituto Superiore di Sanità, condotti in collaborazione con il Sistema Epidemiologico Integrato dell’Epatite Virale Acuta (SEIEVA), si evidenziano tre periodi caratterizzati da andamenti epidemiologici differenti tra il 2015 ed il 2019:
- Periodo pre-epidemico (gennaio 2015 – luglio 2016): caratterizzato da un’incidenza di 0,5 per 100.000 anni/persona, in cui i fattori di rischio preponderanti sono stati il consumo di frutti di mare ed i viaggi in aree endemiche. Livello endemico di base per l’Italia.
- Periodo epidemico (agosto 2016 – dicembre 2017): caratterizzato da un’incidenza di 5,4 per 100.000 anni/persona, in cui è stata rilevato un importate aumento dei casi specialmente tra i maschi che fanno sesso con maschi (MSM); è rimasta alta la trasmissione legata al consumo di frutti di mare ed ai viaggi (in questo caso, però, in aree non considerate endemiche).
- Periodo post-epidemico (gennaio 2018 – dicembre 2019): caratterizzato da un’incidenza di 1,2 per 100.000 anni/persona, con un’importante riduzione dei casi tra i MSM ed un aumento della trasmissione legata ai viaggi in aree endemiche, specialmente in Marocco.
Da sottolineare l’età mediana molto bassa dei soggetti interessati (10-12 anni).
In Italia, il numero di casi nel 2020 (97) si è ridotto rispetto all’anno precedente. È difficile attualmente stabilire se questa riduzione dei casi sia legata più alle misure di contenimento adottate in seguito alla crisi sanitaria causata da Covid-19 o ad un rallentamento diagnostico legato alla pandemia stessa.
L’epatite A non è clinicamente distinguibile dalle altre forme di epatite acuta; la diagnosi avviene mediante la ricerca di IgM specifiche anti-HAV.
Non esiste trattamento specifico; va prestata attenzione al controllo dei sintomi ed al mantenimento dell’equilibrio idrico e nutrizionale; in assenza di insufficienza epatica che richieda l’ospedalizzazione, la gestione dei pazienti è quindi a carico del MMG.
Sono ormai da tempo disponibili diversi vaccini contro l’HAV (in Italia ben due), capaci di garantire protezione già dopo 14-21 giorni; la vaccinazione è particolarmente raccomandata per:
- Viaggi in zone endemiche.
- Tossicodipendenti.
- Contatti familiari di soggetti affetti da epatite A.
- Omosessuali maschi.
- Pazienti affetti da malattie epatiche croniche.
Appare evidente la centralità delle campagne vaccinali nelle strategie di prevenzione dell’Epatite A: nel 2017 sono state decisive per l’interruzione della catena contagi e la rapida decrescita dei casi osservati tra i MSM e nel successivo biennio post-epidemico l’aumento dei casi tra chi non aveva completato il ciclo vaccinale (sia tra i soggetti di ritorno dalle aree endemiche, sia tra i casi secondari) ha evidenziato come circa un terzo dei casi si sarebbero potuti prevenire mediante vaccinazione.
Ugualmente fondamentali rimangono anche le norme igieniche per la prevenzione delle infezioni oro-fecali (igiene personale, lavaggio e cottura degli alimenti a rischio e controllo della coltivazione e della commercializzazione dei frutti di mare).
|
HOT TOPIC |
| · Recente epidemia di Epatite A in Europa e specialmente in Italia, tra il 2016 ed il 2017.
· Riduzione dei casi durante la pandemia: misure di contenimento o rallentamento diagnostico? · Ricerca dei soggetti a rischio: MSM e popolazione proveniente dalle zone endemiche. · La vaccinazione al centro delle strategie di prevenzione. |
HBV
Sono 296 milioni i portatori stimati nel mondo di epatite B cronicizzata, con 1,5 milioni nuove infezioni ogni anno e 820000 decessi stimati nel 2019. In Italia nel 2020 sono stati segnalati 106 nuovi casi di epatite B acuta (incidenza minore rispetto al 2019); più colpito è il sesso maschile.
La forma acuta di epatite B non desta generalmente preoccupazioni (spesso asintomatica; può manifestarsi con nausea, vomito, ittero e febbre di lieve entità dopo un periodo di incubazione generalmente di 60-90 giorni); HBV può però causare infezioni croniche e determinare un aumentato rischio di cirrosi e tumori epatici, complicanze che possono essere evitate grazie al vaccino che dà una protezione che va dal 98 al 100% nei soggetti a cui è somministrato.
L’infezione contratta in età adulta porta alla cronicizzazione in meno del 5% dei casi; se contratto in età neonatale o nell’infanzia si cronicizza nel 95% dei casi: questo spiega ancora meglio l’importanza di una corretta campagna vaccinale.
L’infezione cronica da HBV è un processo dinamico che dipende dalla virulenza del patogeno e dalla risposta immunitaria dell’ospite.
Soggetti particolarmente a rischio sono:
- Tossicodipendenti.
- Soggetti sottoposti a pratiche che prevedano l’uso di aghi e siringhe non sterilizzati (tatuaggi, piercing, manicure, ecc..).
- Operatori sanitari a contatto con persone infette e lavoratori a contatto con l’agente infettivo.
- Contatti familiari e sessuali di persone infette.
L’HBV può essere trasmesso per via parenterale (attraverso il sangue e i suoi derivati) oppure per trasmissione sessuale o perinatale ed ha quindi le stesse vie di trasmissione dell’HIV. Attualmente la maggior parte dei casi di infezione nei paesi industrializzati sono soprattutto i rapporti eterosessuali, nei quali i fattori associati all’aumento del rischio di infezione sono la durata dell’attività sessuale, il numero di partner, una storia di malattie sessualmente trasmesse e l’eventuale presenza di sifilide. L’uso del preservativo impedisce il trasmettersi dell’infezione.
I figli di madri infette con elevati livelli di replicazione virale (caratterizzati da elevati livelli di HBV-DNA e da HbeAg positività), hanno un rischio del 70-90% di infezione perinatale (alla nascita) in assenza di prevenzione. Al contrario, il rischio di trasmissione madre-figlio da madri HbeAg negative è inferiore (10-30%).
La nuova nomenclatura descrive due principali condizioni nel contesto della cronicità da HBV: infezione ed epatite, in relazione alla presenza di HBsAg, HBVeAg, HBV DNA, ALT e alterazioni del parenchima epatico (necroinfiammazione e fibrosi).
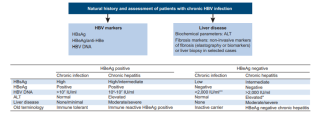
EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection European Association for the Study of the Liver
Nell’infezione cronica HBsAg è positivo, gli anticorpi anti-HBsAg sono negativi, mentre HBeAg può essere sia positivo sia negativo. Si distinguono 5 fasi di cronicità:
- Infezione cronica HBeAg positivo.
- Epatite cronica HBeAg positivo.
- Infezione cronica HBeAg negativo.
- Epatite cronica HBeAg negativo.
- Fase cronica di infezione occulta HBsAg negativo con anticorpi anti-HBc positivo e possibilità di sviluppare anticorpi anti-HbsAg.
I pazienti in fase 3 con infezione cronica che sviluppano anticorpi anti HBeAg erano in passato definiti “portatori inattivi”. In questi pazienti i livelli nel siero di HBsAg sono bassi (<1.000 UI/ml) e c’è un minor rischio di sviluppare cirrosi ed epatocarcinoma. La perdita di HBsAg e/o la sieroconversione può verificarsi in questi pazienti spontaneamente nell’1-3% dei casi per anno.
L’obiettivo nei pazienti con epatite cronica consiste nel sopprimere a lungo termine il genoma virale, consentendo la normalizzazione delle transaminasi. L’induzione della perdita di HBeAg, con o senza sieroconversione anti-HBeAg, rappresenta un parziale controllo immunitario dell’infezione cronica da HBV. La perdita di HBsAg, con o senza sieroconversione anti-HBsAg, rappresenta l’endpoint ottimale, poiché indica una profonda soppressione della replicazione dell’HBV e dell’espressione delle proteine virali.
Nella pratica il MMG invia allo specialista ai fini di iniziare il trattamento:
- Tutti i pazienti con infezione cronica HBeAg positivi/negativi con HBV-DNA>2000 IU/ml, ALT>40 IU/l e segni di necroinfiammazione e/o fibrosi moderata.
- Tutti i pazienti con HBV-DNA >20000 UI/ml e ALT >2ULN indipendentemente dalla presenza di fibrosi.
- Tutti i pazienti cirrotici indipendentemente dai livelli di HBV-DNA e ALT.
Buona norma inviare allo specialista anche:
- I pazienti con HBeAg positivo, genoma dosabile e transaminasi nella norma.
- I pazienti con infezione cronica HBeAg positivo/negativo e storia familiare di cirrosi e/o epatocarcinoma e manifestazioni extraepatiche.
I pazienti cronici che non vengono sottoposti a terapia devono seguire un attento follow up da parte del MMG con la collaborazione eventuale dello specialista:
- In pazienti con infezione cronica, HBeAg positivo, transaminasi di norma e genoma non dosabile, eseguire ALT ogni 3 mesi e HBV-DNA ogni 6-12 mesi e valutazione della fibrosi epatica una volta all’anno.
- In pazienti con infezione cronica HBeAg negativo e con HBV-DNA < 2000 IU/ml, eseguire ALT ogni 6-12 mesi. Importante valutare HBV-DNA e la fibrosi epatica almeno ogni 2 anni se HbsAg > 1000 IU/ml, ogni 3 anni se HBsAg <1000 IU/ml.
- I pazienti con infezione cronica, HBeAg negativo e HBV-DNA >2000 IU/ml, che non vengono sottoposti a terapia, necessitano uno stretto monitoraggio dosando ALT ogni 3-6mesi con controllo annuale di HBV-DNA e della fibrosi epatica.
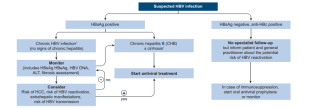
EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection European Association for the Study of the Liver
|
HOT TOPIC |
| · Riduzione dei casi durante la pandemia: misure di contenimento o rallentamento diagnostico?
· Infezione cronica ed epatite cronica: due diverse condizioni cliniche e laboratoristiche. · Follow up della cronicità a carico del MMG e criteri per l’invio allo specialista ben definiti. · End-point ottimale: negativizzazione HbsAg con o senza sieroconversione anti-HbsAg. |
HCV
Sono 54 milioni i portatori stimati nel mondo di epatite C cronicizzata, con 1,5 milioni nuove infezioni ogni anno e290000 decessi stimati nel 2019. In Italia anche l’incidenza dell’epatite C nel 2020 è in calo rispetto all’anno precedente: 19 nuovi casi.
HCV causa infezioni sia acute che croniche: le infezioni acute decorrono solitamente asintomatiche. Circa il 30% dei pazienti infetti elimina spontaneamente il virus entro 6 mesi dall’infezione senza trattamenti. Il restante 70% delle persone svilupperà un’infezione cronica da HCV, in questa categoria il rischio di cirrosi varia dal 15% al 30% entro 20 anni.
Il periodo di incubazione per l’epatite C varia da 2 settimane a 6 mesi. La maggior parte delle persone infettate risultano asintomatiche: qualora invece vengano sviluppati sintomi, essi possono essere febbre, affaticamento, diminuzione dell’appetito, nausea, vomito, dolore addominale, urine scure, feci pallide, dolori articolari e ittero.
La trasmissione del virus C è prevalentemente per via ematica; rappresentano quindi una via comune di contagio:
- La trasfusione di sangue ed emoderivati non selezionati.
- L’uso di dispositivi sanitari non adeguatamente sterilizzati (soprattutto nei paesi in via di sviluppo).
- L’uso di strumenti per piercing e tatuaggi non sterilizzati.
- L’uso promiscuo di aghi per l’iniezione di droghe per via endovenosa.
Altre vie di trasmissione sono rappresentate dalla trasmissione verticale-perinatale della madre al suo bambino (rischio maggiore nei casi di madri con infezione concomitante da HIV) e da pratiche sessuali, seppur in misura inferiore rispetto al virus dell’epatite B.
Dato che la maggior parte delle infezioni decorre senza sintomi, la diagnosi di un’infezione recente è rara, spesso viene scoperta dopo diverso tempo in seguito allo sviluppo di un danno epatico.
Per la diagnosi è importante il test sierologico per la ricerca degli anticorpi anti-HCV, che permette l’identificazione delle persone che sono state infettate dal virus; qualora il test sierologico dia risultato positivo, poiché gli anticorpi non indicano necessariamente un’infezione in atto ma possono risultare positivi anche diverso tempo dopo la guarigione (sia spontanea che dopo terapia), bisognerà andare a cercare l’RNA virale. Se confermata la presenza dell’RNA virale sarà opportuno la determinazione genotipica: sono infatti sei i principali genotipi del virus dell’epatite C, che rispondono in modo variabile al trattamento. Il genotipo 1 è più comune in Italia.
Qualora si riscontrasse la presenza dell’infezione è opportuno andare a valutare il grado di danno epatico attraverso l’elastografia, preferita alla biopsia per la minor invasività.
L’infezione da HCV si può curare.
Da alcuni anni è disponibile una nuova classe di farmaci: i DAA (antivirali ad azione diretta) che hanno un tasso di efficacia prossimo al 100%. Nonostante l’alto tasso di guarigione, le terapie antivirali di nuova generazione riducono, ma non azzerano il rischio di sviluppare un epatocarcinoma nei pazienti cirrotici (riduzione della mortalità globale, dell’incidenza di HCC e della mortalità da HCC comunque in netta riduzione), perciò il follow-up ecografico ogni 6 mesi rimane indicato.
I DAA sono efficaci nella maggior parte dei pazienti con infezione da HCV e trovano indicazione a partire dai 12 anni. La durata del trattamento è breve (di solito da 12 a 24 settimane), a seconda dell’assenza o della presenza di cirrosi.
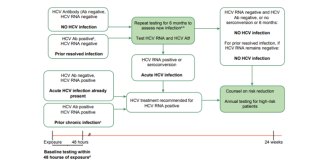
Hepatitis C Guidance 2019 Update: AASLD-IDSA (Infectious Diseases Society of America) recommendations for testing, managing, and treating hepatitis C virus infection
Attualmente non esiste un vaccino efficace contro l’epatite C; la prevenzione dipende dalla riduzione del rischio di esposizione al virus negli ambienti sanitari e nelle popolazioni a rischio più elevato.
Con la pubblicazione in Gazzetta Ufficiale del Decreto del ministro della Salute di concerto con il ministro dell’Economia e delle Finanze “Esecuzione dello screening nazionale per l’eliminazione del virus dell’HCV” del 08/07/2021, si attiverà nel nostro Paese lo screening nazionale gratuito contro l’epatite C.
Il decreto definisce i criteri e le modalità per l’attuazione dello screening da parte delle Regioni e stabilisce che sia rivolto, in via sperimentale, a:
- Tutta la popolazioneiscritta all’anagrafe sanitaria nata dal 1969 al 1989, inclusi gli stranieri temporaneamente presenti.
- Soggetti seguitidai servizi pubblici per le Dipendenze (SerD) e ai detenuti, indipendentemente dalla coorte di nascita e dalla nazionalità.
Lo screening dell’infezione attiva dell’HCV è effettuato con l’intento di rilevare le infezioni da virus dell’epatite C ancora non diagnosticate, migliorare la possibilità di una diagnosi precoce, avviare i pazienti al trattamento onde evitare le complicanze di una malattia epatica avanzata e delle manifestazioni extraepatiche, nonché interrompere la circolazione del virus impendendo nuove infezioni.
|
HOT TOPIC |
| · Riduzione dei casi durante la pandemia: misure di contenimento o rallentamento diagnostico?
· Test sierologico centrale nella diagnosi di epatite C; se positivo si ricerca RNA virale. · DAA efficaci nella cura dell’epatite C; rimane comunque indicato FU ecografico ogni 6 mesi. · Sarà presto avviato il progetto di screening nazionale gratuito contro l’epatite C. |
HDV
A livello globale HDV infetta circa il 5% dei pazienti affetti da epatite B cronica. Il numero complessivo di infezioni da HDV risulta comunque in forte calo rispetto a trenta anni fa.
HDV è considerato un subvirione che necessita della concomitante presenza di HBV per poter infettare le cellule epatiche. L’infezione può verificarsi secondo due modalità:
- Infezione simultanea di HDV ed HBV: epatite clinicamente simile all’epatite B.
- Sovrainfezione di HDV in un portatore cronico di HBV: epatite acuta, a volte anche fatale.
In entrambi i casi l’infezione può cronicizzare: la coinfezione da HDV-HBV è considerata la forma più grave di epatite virale cronica a causa della più rapida progressione verso un danno epatico grave, con la comparsa di cirrosi ed epatocarcinoma.
La modalità di trasmissione è la stessa dell’epatite B e il periodo di incubazione va da 2 a 8 settimane.
Anche in questo caso, per la diagnosi è necessaria la ricerca di immunoglobuline specifiche IgM ed IgG; la presenza di HDV-RNA conferma l’infezione in atto. Purtroppo, questi test non risultano sempre di facile disponibilità.
Attualmente la terapia prevede l’uso di INF-α pegilato, che garantisce purtroppo scarsi risultati ed importanti effetti collaterali; nuove terapie basate sull’utilizzo di farmaci biologici sono ancora in fase di studio.
Per quanto riguarda le misure preventive, vale la profilassi per l’HBV; il vaccino contro l’epatite B è quindi in grado di proteggere anche contro l’epatite D.
|
HOT TOPIC |
| · Netta riduzione dei casi di epatite da HDV negli ultimi trenta anni.
· La coinfenzione da HDV-HBV è considerata la forma più grave di epatite virale cronica. · Non sono ancora disponibili terapia specifiche contro HDV. · Il vaccino contro l’epatite B protegge anche dal rischio di sviluppare epatite da HDV. |
HEV
Secondo l’OMS ogni anno, nel mondo, circa 20 milioni di persone contraggono l’infezione del virus HEV e, nel 2015, circa 44 mila persone sono morte per epatite fulminante correlata a questo virus.
In Italia, dal 2017 al 2019, si è assistito ad un trend in continuo aumento; nel 2019 è stato raggiunto un vero e proprio picco con un numero di casi raddoppiato rispetto al 2018 (102). Anche nel 2020, nonostante una netta riduzione dei casi registrati (24), le diagnosi di epatite da HEV hanno superato quelle di epatite da HCV.
HEV, dopo un periodo di incubazione di 15-64 giorni, causa un’infezione solitamente anitterica, autolimitante; in rari casi può evolvere in forme cliniche fulminanti, soprattutto nelle donne incinte, negli anziani e nei pazienti con epatopatie preesistenti.
Casi di cronicità sono riportati solamente in pazienti immunocompromessi.
Come per l’epatite A, la trasmissione avviene per via oro-fecale, e l’acqua contaminata da feci è il veicolo principale dell’infezione.
Epidemie e casi sporadici sono stati registrati principalmente in aree geografiche con livelli igienici inadeguati. Nei Paesi industrializzati, la maggior parte dei casi riguarda persone di ritorno da viaggi in Paesi endemici; sono tuttavia in aumento i casi autoctoni (come dimostra quanto successo in Italia nel 2019).
Per la diagnosi è necessaria la ricerca di immunoglobuline IgM specifiche anti-HEV; clinicamente non è distinguibile dalle epatiti acute di altra natura.
Non esiste uno specifico trattamento e l’ospedalizzazione è necessaria solo nelle forme fulminanti, ma dovrebbe essere anche considerata per le donne in gravidanza sintomatiche. Per i pazienti immunocompromessi si sono dimostrati efficaci farmaci antivirali come la ribavirina.
La prevenzione rimane l’arma migliore contro l’HEV; i casi di epatite possono essere ridotti rafforzando le norme igieniche per la prevenzione delle infezioni oro-fecali:
- Assunzione di acqua potabile.
- Controllo delle acque pubbliche.
- Attenzione nell’assunzione di carne poco cotta di animali infetti (suini, selvaggina, ecc…).
Sono in corso studi clinici sperimentali per la commercializzazione di due vaccini (la vaccinazione è attualmente disponibile solo in Cina).
È stata inoltre proposta la somministrazione di gammaglobuline, soprattutto nelle donne gravide, ma la loro efficacia deve essere dimostrata.
|
HOT TOPIC |
| · In Italia, nel 2020, i casi di epatite causati da HEV hanno superato quelli causati da HCV.
· Raramente può evolvere in forme fulminanti; cronicizza solo in pazienti immunocompromessi. · Per i pazienti immunocompromessi dimostrata l’efficacia di farmaci antivirali (es. ribavirina). · Prospettive: in corso studi su due vaccini; attualmente vaccino disponibile solo in Cina |
BIBLIOGRAFIA
- salute.gov.it/portale
- epicentro.iss.it/epatite/epatite
- who.int/health-topics/hepatitis#tab=tab_1
- Maria Elena Tosti, Annamaria Mele, Luigina Ferrigno et al. L’epatite A in Italia negli ultimi cinque anni: dati della Sorveglianza SEIEVA 2015-2019. Not Ist Super Sanità 2021;34(6):8-12
- Ndumbi P, Freidl GS, Williams CJ, et al. Hepatitis A outbreak disproportionately affecting men who have sex with men (MSM) in the European Union and European Economic Area, June 2016 to May 2017. Euro Surveill 2018;23(33):1700641.
- Tremolada S, Delbue S, Ferrante P. Infezioni virali congenite, perinatali e neonatali [Viral infections of the fetus and newborn infant]. Pediatr Med Chir. 2008;30(4):177-191.
- European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol. 2017 Aug;67(2):370-398.
- Ghany MG, Morgan TR; AASLD-IDSA Hepatitis C Guidance Panel. Hepatitis C Guidance 2019 Update: American Association for the Study of Liver Diseases-Infectious Diseases Society of America Recommendations for Testing, Managing, and Treating Hepatitis C Virus Infection. 2020 Feb;71(2):686-721.
- Loreta Kondili, Maria Giovanna Quaranta,Luigina Ferrigno et al. Eliminazione dell’epatite C cronica in Italia: strategie di screening gratuito. Not Ist Super Sanità 2021;34(1):3-8.
- Legge n. 8, 28 febbraio 2020. Articolo 25 sexies – Screening nazionale gratuito per l’eliminazione del virus HCV. Gazzetta Ufficiale n. 51, 29 febbraio 2020, Supplemento ordinario n. 10.
- cdc.gov/hepatitis/hdv/index.htm
- Farci P, Niro GA. Current and future management of chronic hepatitis D. Gastroenterol Hepatol 2018;14(6):342–51
- European Association for the Study of the Liver. European Association for the Study of the Liver. EASL Clinical Practice Guidelines on hepatitis E virus infection. J Hepatol. 2018 Jun;68(6):1256-1271.
- Patra S, Kumar A, Trivedi SS, Puri M, Sarin SK. Maternal and fetal outcomes in pregnant women with acute hepatitis E virus infection. Ann Intern Med. 2007 Jul 3;147(1):28-33.
A cura di:
Rosa Nevola – Area Scientifica FIMMG Formazione Piemonte
Vittorio Picottino – Referente Area Scientifica FIMMG Formazione Piemonte
Fabio Sirianni – Area Scientifica FIMMG Formazione Piemonte